2017年4月6日,生物领域Nature子刊《Nature Protocols》在线发表了我院刘震教授研究团队关于分子印迹领域的重要论文“Preparation of molecularly imprinted polymers specific to glycoproteins, glycans and monosaccharides via boronate affinity controllable-oriented surface imprinting”(Nature Protocols, 2017, 12, 964-987. doi:10.1038/nprot.2017.015)。
分子印迹是制备具有类似抗体或酶专一性仿生识别材料的重要技术,在生物传感、亲和分离和疾病诊断等领域具有广阔的应用前景。但是,蛋白质等生物分子的普适、高效印迹是分子印迹中的一个重要的挑战,传统方法难以同时满足不同大小的生物分子的印迹,更难以对印迹过程进行精确控制。经过多年在硼亲和材料(Chem. Soc. Rev. 2015, 44, 8097-8123; Angew. Chem. Int. Ed., 2009, 48, 6704-6707; 2015, 54, 6173-6176; Chem. Sci., 2012, 3, 1467-1471; 2013, 4, 4298-4303; 2014, 5, 4065-4069)和分子印迹(Angew. Chem. Int. Ed., 2013, 52, 7451-7454; 2014, 53, 10386-10389; 2015, 54, 10211-10215 (VIP); Chem. Sci., 2014, 5, 1135-1140;Anal. Chem., 2016, 88, 1447–1454 (ACS Editors' Choice))领域中的深入研究,该研究团队发展出硼亲和可控定向表面印迹法。该方法能够便捷高效地制备出糖蛋白、聚糖和单糖的分子印迹聚合物。该方法的原理见图1,先将模板分子固定到硼酸功能化的基质上,然后利用生物相容性良好的功能单体在基质表面聚合,形成合适厚度的印迹层以及与模板分子空间匹配的印迹腔。该方法的最大优势在于印迹可控性:根据模板分子尺寸大小,调整印迹层厚度,制备出不同尺寸模板的分子印迹聚合物,而印迹层厚度只需要调节印迹时间来精确控制。这不仅简化了印迹步骤,而且适用范围广。所得分子印迹聚合物已经在疾病诊断(Anal. Chem., 2014, 86, 959-966;2014, 86, 12382-12389;2016, 88, 12363-12370)、癌细胞靶向识别(Chem. Commun., 2015, 51, 17696- 17699;Sci. Rep., 2016, 6, 22757)和活体单细胞分析(Angew. Chem. Int. Ed., 2016, 55, 13215-13218)等重要应用领域中展现出优越的分子识别性能。
该论文的共同第一作者为博士生邢荣荣和博士后王双寿。该工作得到国家杰出青年科学基金、国家自然科学基金面上项目和国家重大科学研究计划(973计划)的经费支持。
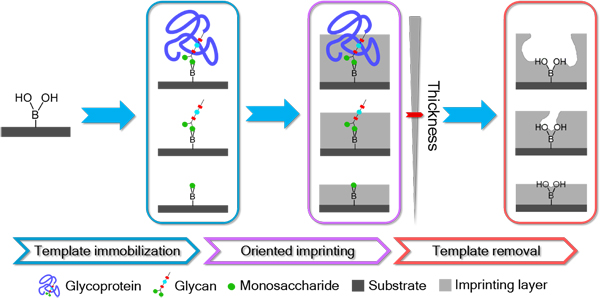 图1. 硼亲和可控定向表面印迹原理
|
